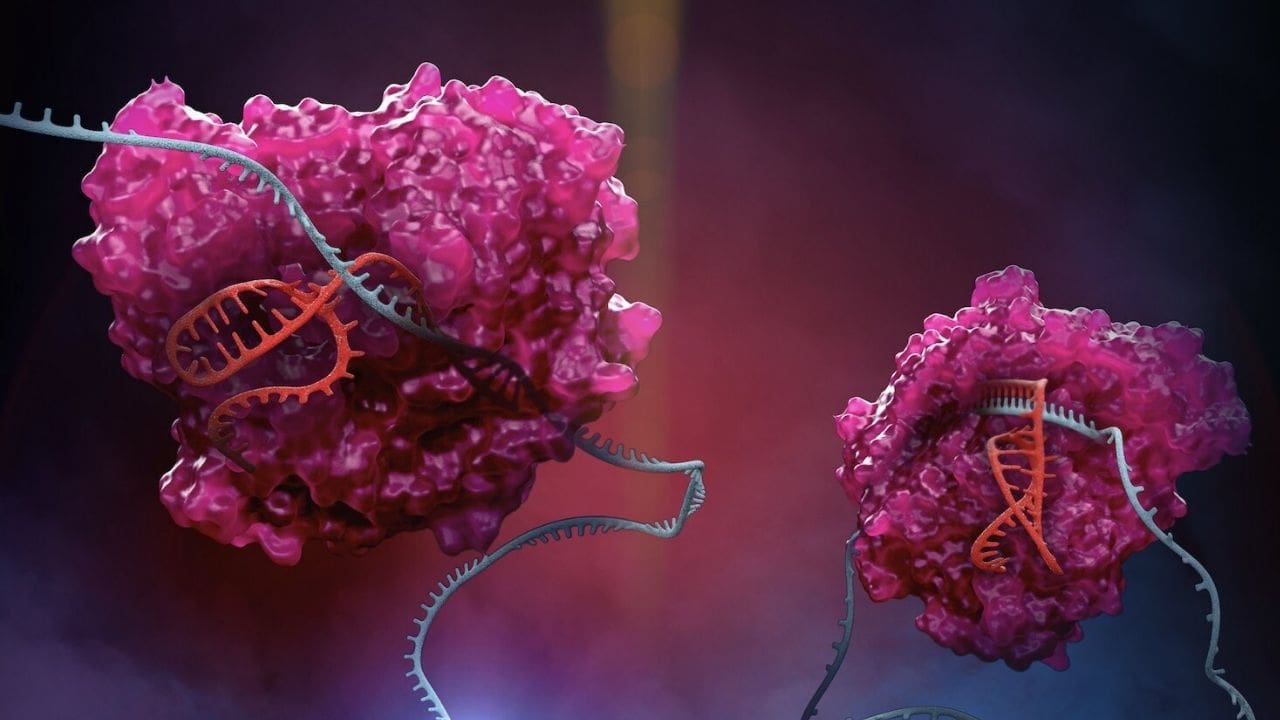
Bilimin her alanında önemli gelişmeler yaşanıyor. Çağımız her bir araştırmanın çürütüldüğü gibi daha farklı boyutlarla ele alındığı ve muazzam ötesi sonuçların elde edilebildiği bir çağ. İnsanın en küçük yapı taşının bugün bize verdiği cevaplar bir zamanlar hayal bile edilemezken, günümüzde o cevaplar bile yeterli gelmiyor. Genlerimiz, bizi biz yapan, atalarımızdan milyonlarca yıl öncesinde bile bize izler bırakan muazzam yapılar. Peki, günümüzde gen teknolojisi ne durumda? Bu anlamda yapılan çalışmalar neler?
Ortalıkta birçok bilgi kirliliği mevcut. Genetiği değiştirilmiş gıdalar, aşılar, gen tedavileri, süper bebekler, yapay etler… Her önüne gelenin kamera karşısına geçip herhangi bir sosyal platformda kulaktan dolma ya da sahte bilgilerle açıklama yapmalarından biz sıkıldık. Genetik alanında doğru bildiğimiz yanlışlar, öğrenmemiz gerekenler neler ve çağın önemli olaylarından biri olan CRISPR ne demek? Moleküler biyoloji alanında Türkiye’de önemli başarılar elde eden Araştırma Görevlisi Dr. Burak Berber‘e sorduk, kendisi tüm açıklığıyla cevap verdi. Haydi hep birlikte, genlerimize odaklanalım.

CRISPR nedir? Hangi alanlarda kullanılıyor?
Açılımı Clustered Regularly Interspaced Short Palindromic Repeats (Kümelenmiş aralıklı pandromik tekrar dizeleri) olan bir mekanizmanın keşfedilmesi ile ortaya çıkmış gen düzenleme aracıdır. İsmi karmaşık gelebilir, okuyucularımız için bunu basitleştirerek anlatmak gerekirse bakteri DNA’sının içerisinde tespit edilen tekrarlayan dizeler olarak isimlendirebiliriz. Bu tekrarlayan bölgelerin tam olarak nasıl bir işlevi olduğu son 20 yılda açığa çıkartılmış olup, 2020 yılında Emmanuel Charpentier ve Jennifer Doudna bu mekanizmayı kullanarak geliştirdikleri yeni gen düzenleme metoduyla birlikte Nobel ödülü aldı.
Peki, nasıl bir mekanizma ki bu, gen düzenlemede kullanılıyor?
Aslında bakterilerin kendilerini enfekte eden bakteriyofajlara (bakteri enfekte eden virüs) karşı geliştirdikleri bir savunma mekanizması. CRISPR sistemi Cas adını verdiğimiz enzimlerle birlikte çalışır. Cas enzimleri bu tekrarlayan dizilerde bakteriyofajlardan kesilerek bakteri DNA’sına eklenen parçaları taşır ve eğer yeniden bu bakteriyofaj türü karşısında enfekte olursa bu enzimler o faj DNA’sını tanıyacak ve keserek yok edecektir. Bu sayede bakteri bu faj türüne karşı savunma kazanmış oluyor. Biraz daha mekanizmanın keşif sürecine değinecek olursak Donisco yoğurt fabrikasında çalışan Rodolphe Barrangou, Ph.D’dan bahsetmemiz gerekir.
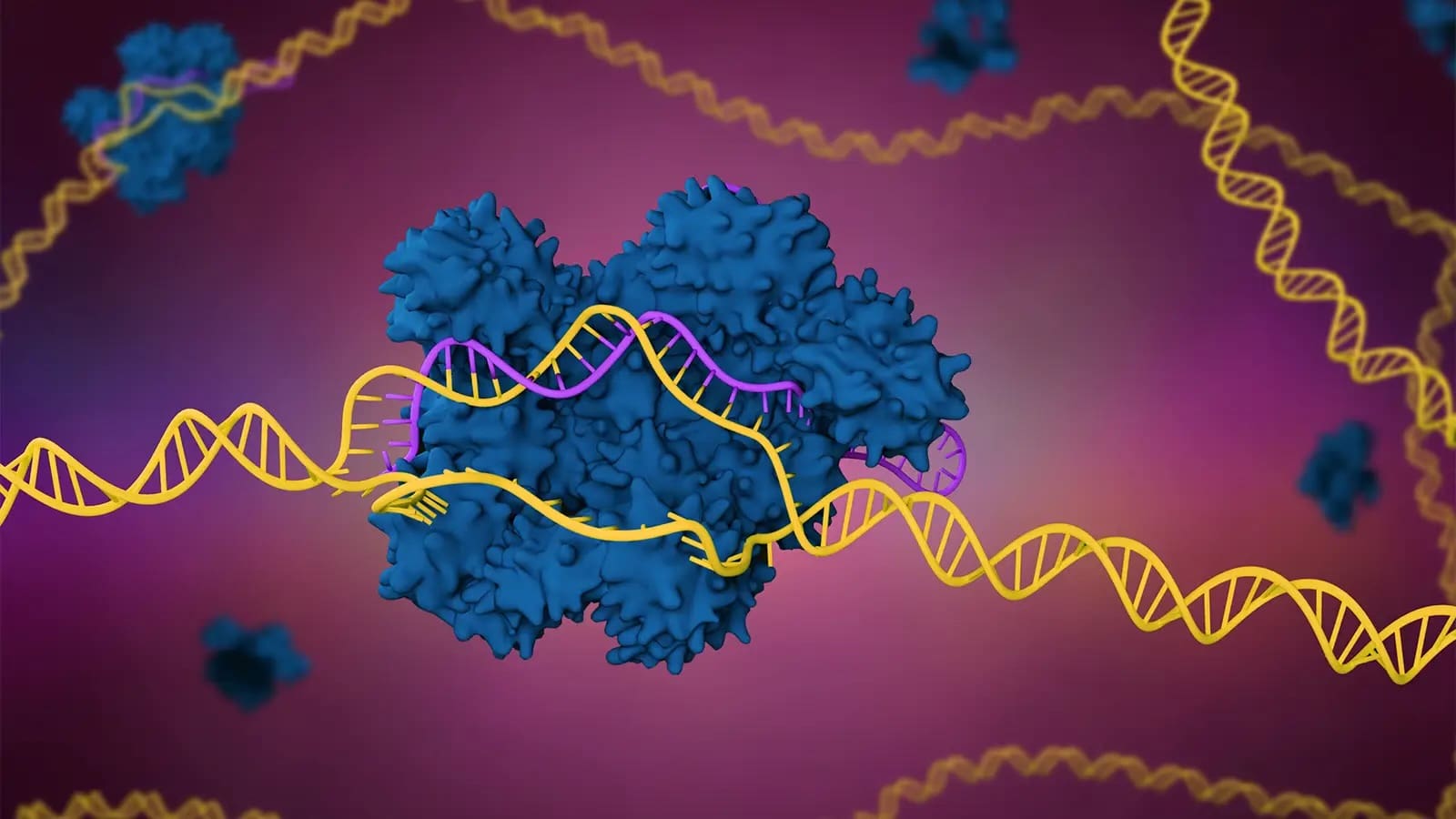
YOĞURT FABRİKASINDA TEMELLERİ ATILDI
Yoğurt fabrikasında keşfedildi demeyin…
Evet, kendisi daha iyi yoğurt elde edebilmek üzere araştırmalar yaparken yoğurtların daha kaliteli mayalanabilmesi için mayalama işleminde kullanılan bakterilerin bakteriyofajlara karşı daha dirençli hale gelmesi gerektiğini düşünerek araştırmalar gerçekleştirmiştir. Yaptığı çalışmalar CRISPR’ın keşfinde önemli rol oynamıştır. Enfekte ettiği bakteryofaj türlerine karşı direnç kazanan bakterilerde genomlarında tekrarlayan dizelerin arttığını ve bu tekrarlayan dizelerin arasında enfekte eden bakteriyofajlara ait dizi bilgileri bulunduğunu tespit etmiştir. Jennifer Doudna ve Emmanuel Charpentier’ın keşfinde bu bilgi oldukça önemli rol oynamıştır. Jennifer ve Emmanuel bu sistem içerisinde kullanılan Cas enzimini üreterek istenilen gen bölgesinin bu enzime yerleştirilmesiyle hedeflenilen gen bölgesinin kesiminin başarılı bir şekilde gerçekleştiğini ortaya koymuştur. Cas enzimlerinin bir çok farklı türü var. CRISPR-Cas9 diye ifade edilmesinin nedeni Cas9 enziminin o dönemde en etkin aktiviteyi göstermesi ve kullanılmasından ötürü idi. Şu an gen düzenleme çalışmalarında Cas13 de oldukça yaygın kullanılmaya başlanmıştır. Genom dizilimini bildiğiniz organizmalar da istediğiniz gen bölgesine müdahale etme imkanı sunuyor size. Ayrıca bu noktada Feng Zhang’dan da bahsetmemiz gerekir. Kendisinin geliştirdiği mekanizma sayesinde CRISPR-Cas sistemi insan hücrelerinde de kullanılabilir hale gelmiştir. Günümüzde bitki, hayvan, insan çalışmaları gerçekleştirilmektedir.
BİR GEN HASARI 1 İLA 6 AY ARASINDA TESPİT EDİLİYOR
Gen hasarlarının sebepleri neler?
Gen hasarlarını genin işlevini bozan değişimler olarak dile getirebiliriz. Gen’den aracı bir molekül olan mRNA üretilir ve mRNA sayesinde protein oluşur. Eğer gen diziliminde hatalı bir bölge oluşursa protein doğru şekilde oluşmaz ve hücre içi işlevlerde bozukluklara neden olabilir. Bu yapısal değişimler, çevresel, kalıtımsal faktörlere göre etkilenebilir.
Bir hasarlı genin tespit edilmesi ne kadar süre alıyor?
Hasarlı geni tespit etmek kolay bir süreç değil günümüzde. Doğru tanı ve teşhisle ortaya çıkarılabilir. Şu anda gerçekleştirilen çalışmalar daha çok hastalığa neden olan mutasyonların daha önce bildirilmiş olması. Bu mutasyona sahip benzer bulgulara rastlanan hastaların verilerine göre ilerleniyor. Hastadan alınan kan örneği ya da doku örneğinden tüm genom sekanslama ya da tüm ekzom sekanslama analizleri yapılarak hastalığa sebebiyet verebilecek, geçmişte bildirilmiş hasarlı bir gen olup olmadığına biyoinformatiksel analizlerle bakılıyor. Ülkemizde henüz çok hızlı şekilde bu analizleri gerçekleştiremiyoruz. 1 ay ile 6 ay arasında sonuç verilebiliyor. 6 aydan daha uzun sürede rapor edilen bölgeler olduğunu da biliyorum.

ÖZEL TASARLANMIŞ VİRÜSLERLE TEDAVİ
Şu an uygulanan gen tedavileri neler?
B-Talasemi (ZYNTEGLO), SMA (Zolgensma), B-Hücre Lenfoma (YESCARTA, TECARTUS), distrofik epidermolizis bülloza (COL7A1 gen mutasyonları-VYJUVEK), serebral adrenolökodistrofi (ABDC1 geni mutasyonu, SKYSONA), hemofili A (ROCTAVIAN), RPE65 mutasyonu ilişkili- retinal distrofi (LUXTURNA) gibi FDA tarafından onaylanmış gen tedavileri mevcuttur. Genel olarak kan hastalıklarıyla ilişkili genetik tedaviler, kan hücrelerinin kolay bir şekilde elde edilip, kültüre edilebilmesi nedeniyle diğer dokusal hastalıklara göre daha elverişlidir. Kan hücrelerinde genetik düzenlemeyi yapıp tekrar kişiye geri enjekte ederek, bu hücrelerin lenfoma gibi hastalıklarla savaşmasını sağlayabiliyorsunuz. SMA gibi dokuya bağlı genetik düzenlemeler özel tasarlanmış virüslerle gerçekleşiyor. Bu özel tasarlanmış virüsler kendilerini çoğaltamazken gerekli taşınması gereken gen bölgesini ve dokuya spesifisik bağlanma sağlıyorlar. Maalesef günümüzde dokuya spesifik geliştirilmiş virüsler oldukça az olduğu için Zolgensma gibi ilaçlar milyon dolarlara satılıyor.
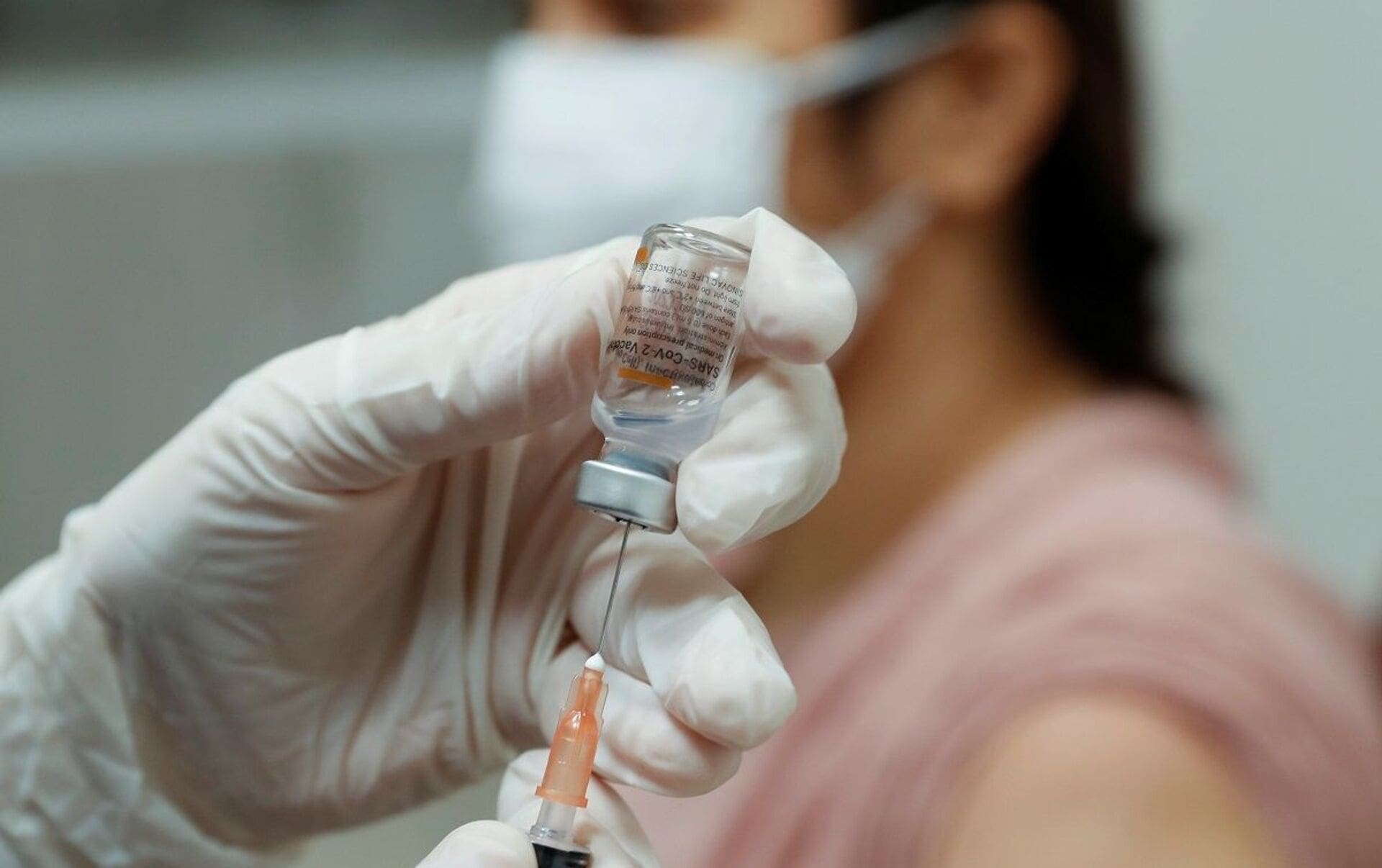
“HER KONUŞANIN DOĞRU KONUŞTUĞUNA İNANIYORUZ”
Dünya koronavirüsle büyük bir pandemi süreci atlattı. Pandemi döneminde geliştirilen tedavilerle ilgili inanılmaz bilgi kirliliği ve çok sayıda spekülasyonlar vardı. Bunlardan en çok dikkatimi çekenlerden biri de “Genetiğimizi değiştirdiler” söylemleriydi. Herhangi bir gene dışarıdan müdahale edilip bu kadar kısa sürede değiştirilebiliyor mu?
Böyle bir durum söz konusu değil kesinlikle. En önemli neden biyoloji bilgimizin bu konuda yetersiz olması. Özellikle Youtube gibi platformlarda her video yayınlayanın ya da spekülatif konuşanın doğru içerik verdiğine inanmamızdan kaynaklanıyor. Belge konularak sunulan iddialar aslında tamamen alakasız. Ancak, bu tip kişileri takip edenler belgelerin peşine düşüp doğruluğunu araştırmıyor. Söylenilene çok kolay inanıyoruz. Bilim insanlarına olan inancın toplumumuzda oldukça azaldığını hissediyorum. Özellikle Prof. Dr. gibi unvanlarla bilim dışı söylemlerde bulunanlar, toplumun bilim insanlarına olan inancını önemli ölçüde kırmış durumda. Bu yüzden de oldukça üzgünüm. Konuya gelecek olursak iki tip aşı geliştirildi pandemi döneminde. İnaktif aşı olarak adlandırılan aşı, bağışıklık hücrelerimizin tanımadığı bu yeni virüs tipinin tanınmasını sağlamak amacıyla kullanılır, virüsün sadece yüzey yapısının izole edilmesiyle oluşturulmaktadır. Virüsün DNA’sı yok edilir. Bu sayede yabancı virüs protein yapısını bağışıklık hücrelerine tanıtılarak bağışıklık hücrelerinin bu yapıyı öğrenmesi sağlanır. Bunun yapılabilmesi için çok fazla virüs proteini üretilmesi gerekir. Pandemi sürecinde sizler de dikkat etmişsinizdir virüs çok fazla mutasyona uğradı. Her mutasyona uğradığında sizin oluşturmuş olduğunuz aşılar artık geçersiz kalma riskiyle karşı karşıya. Çünkü virüs yapısındaki protein şekil değiştiriyor. Yani sizin bağışıklık hücrelerinize öğrettiğiniz protein artık değişti anlamına geliyor bu. İşte bu gibi değişimlere hızlı cevabı yeni nesil mRNA (mesajcı RNA) aşılarıyla verebilirsiniz.
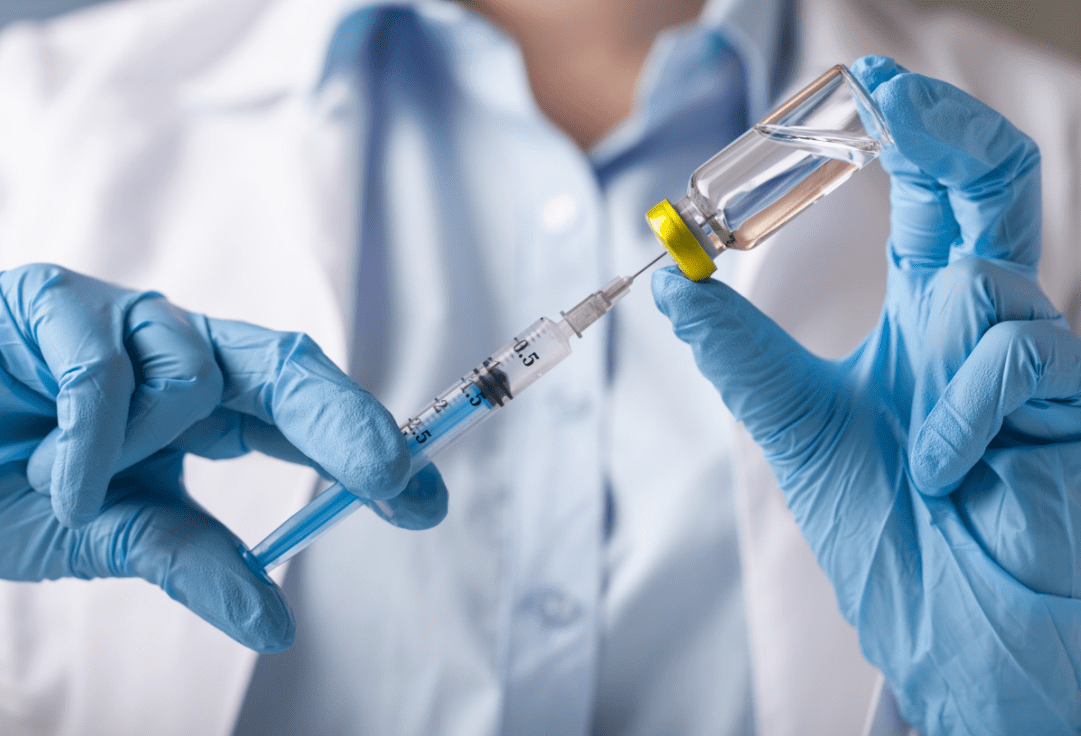
Öncelikle mRNA genoma katılamaz. Yani bu şu demek, mRNA, hücre çekirdeği içerisinden geçip kalıtsal materyal olan genomun içine yerleşemez. mRNA genomumuzda çeşitli genlerin ürünü olarak üretilmesi için gerekli gen şifresini hücre sitoplazmasına taşır. Hücre sitoplazmasında ribozomlar aracılığıyla da protein üretilir. mRNA üzerindeki her bir genetik şifre bir aminoasite karşılık gelir. Örneğin CUA kodlaması lösin aminoasitinin üretilmesini sağlar. Bir diğer husus, mRNA hücre sitoplazmasında çok uzun süre kalamaz degrade olur, parçalanır. mRNA aşılarında virüsün yapısındaki spike protein genetik kodunu içeren mRNA’lar tasarlanarak kişilere enjekte edildi. Kaslarımızdaki hücreler, bağışıklık hücrelerimizin tanıması için bu spike proteinleri ürettiler. Bu geçici bir süreç. Çünkü spike proteinlerin genomda bir bilgisi olmadığı için belli bir süre sonra hücrede yıkılarak yok edilmektedir. mRNA’lar da benzer şekilde çok kısa bir süre sonra işlevini gerçekleştirdikten sonra yok olmaktadır. Vücudumuzda milyarlarca aynı DNA’yı taşıyan hücre var. Genetik bilgimizin değişmesi ihtimal dahilinde bile değil. Sperm hücreleri ve yumurtalar genomumuzun etkilenebileceği en hassas hücrelerdir. Benzer şekilde mRNA genom yapısına katılamadığı için bu hücrelerde de genetiği değiştiremez. CRISPR ile insanlar mRNA aşısını karşılaştırmasınlar. Mekanizma olarak çok farklı olduğu için genom düzenlemeyle alakası bulunmamaktadır. Bu nedenle mRNA aşılarından korkmanın bir anlamı bulunmamaktadır. Spike protein üretiminden hemen sonra kişilerde farklı reaksiyon, beklenmeyen yan etkiler ortaya çıkabilir. Her bir insanın genetiği eşsizdir, farklılıklar içerir. Bu farklılıklardan ötürü kimimiz koronavirüsü kolay atlattık, kimimiz bu yüzden vefat etti. Benzer durum mRNA aşısı sonrasında da gelişen hastalarda düşük oranda oldu. Spike proteinin üretiminin geliştirmiş olduğu yan etkilerden biri kalp krizleri olabilir. Bunun nedeni mRNA aşısı değil virüs proteininin yapısı ve bağışıklık hücrelerinin verdiği yanıttır. Enfekte olan kişilerde de kalp krizlerinde artış olabilmektedir. Bu noktada metabolik etkileşimler, bağışıklık hücrelerinin yanıt gücü, kişinin yaşı, genetik farklılıklar gibi bir çok faktör arka planda rol oynamaktadır. Bu nedenlerle mRNA aşışı kalp krizileriyle doğrudan ilişkili değildir.

HEM YARARLI, HEM ZARARLI
Genetiğiyle oynanmış yani GDO’lu dediğimiz gıda ürünlerinin uzun vadede insan sağlığına zararları neler?
Zararlı olup olmadığını tartışabilmemiz için öncelikle GDO tam olarak nedir anlamaya çalışırsak zararlı olup olmayacağı konusunda konuşabiliriz. GDO’da en temel amaç bitkinin olumsuz koşullara karşı dirençli olmasını sağlayarak, bitkilerin daha verimli olmasını sağlamak. Bunu ne gibi yollarla yaptıklarını soracak olursanız çeşitli örnekler verip sizleri aydınlatmak isterim. En çok bilinen örneklerden biri GDO’lu mısırdır. Örneğin, BT mısır olarak adlandırılan mısırlar, bacillus thuringiensis bakterisinin ürettiği böcek öldürücü endotoksin genini taşıyan mısırlardır. Bu bakterinin böcekleri öldüren endotoksin üretmesine sebep olan genini bilim insanları mısırlara aktararak, Cry1ac olarak belirlenen toksinin üretilmesi sağladılar. Mendelsohn ve arkadaşları 2003 yılında yaptıkları bir derleme çalışmada olası etkilerden bahsetmişler. Bu toksin sadece mısırı hasta eden ya da mısıra zarar veren patojenlere değil aynı zamanda yararlı canlılar için de bir tehlike arz edebiliyor. Bunun olasılığı düşük olarak görülüyor. Ayrıca toprakta kalma süresi de 20-40 gün arasında değişkenlik gösterebiliyor. Bu süreçte toprakta bulunan diğer canlılar da bu toksinlere maruz kalabilir. Ayrıca bu mısırlarla beslenen insanlarda toksine karşı alerjik reaksiyonlar da gelişme olasılığı bulunmaktadır. Ancak, mısır genetiği değiştirildi diye genetiğimizin değişmesi gibi bir durum yine söz konusu değildir. Tabi her GDO’lu ürün toksin üretecek anlamına da gelmesin bu anlattıklarım. Verdiğim örneklerden biri sadece.
Bir diğer önemli patojen bitkiler için virüslerdir. Niraula ve Fondong (2021) yazdıkları derleme makalede bitkileri enfekte eden virüslere karşı bitkilerin genomuna yerleştirilen antiviral gen bölgelerinin insan ya da hayvan sağlığına etki etmediğini, bunun bitkilerin korunması için pozitif bir biyoteknolojik gelişme olduğunu, evrimsel süreçlerde bitkilerin zararlı virüslere karşı kendi bağışıklık sistemlerini benzer yöntemlerle kazandıklarını tartışıyor.

Çin 1999 yılında domatesin Coat protein geni üretmesini sağlayarak, Cucumber Mosaic Virus (CMV)’e karşı dirençli domatesler üretmişlerdir. Bu virüs 1000’den fazla bitki türünü enfekte edebilen ticari açıdan oldukça zarar verici etkilere sahip, etkin virüslerden biridir. Biyoteknolojinin de gelişmesiyle birlikte günümüzde daha da artan sayıda denemeler yapılmakta ve onaylar alınmaktadır. GDO’lu ürünlerin zararlı ya da yararlı olduğuna dair kesin kanıya varmak pek mümkün değil. Araştırmaların kapsamlı bir şekilde devam etmesi gerekiyor. Ülkemiz tohum kaynağı konusunda çok riskli bir dönem içerisindedir. Ülkemize giren her tohum genetik analizden geçirilmeli, referans olarak alacağımız genetik bilgiler de kendi ata tohumlarımızdan olmalıdır. Bu konuda önemli çalışmalar gerçekleştiriliyor olsa da oldukça geride kalmış olmakla birlikte denetim mekanizmalarının sıkılaştırılması sağlığımız açısından önem arz etmektedir. Bahsettiğim üzere GDO’lu ürün demek sadece basit bir etiket. Hangi yöntemle, ne gibi bir genetik modifikasyona uğramış, nasıl bir mekanizma üzerinden etki gösteriyor, toksin üretiyor mu, toksinlerin insan sağlığı üzerindeki etkileri var mı gibi pek çok soruyu kendi yaptığımız deneylerle araştırıp, bu ürünlerin ülkemizde kullanılıp kullanılamayacağına kendimiz karar vermemiz gerekmektedir.
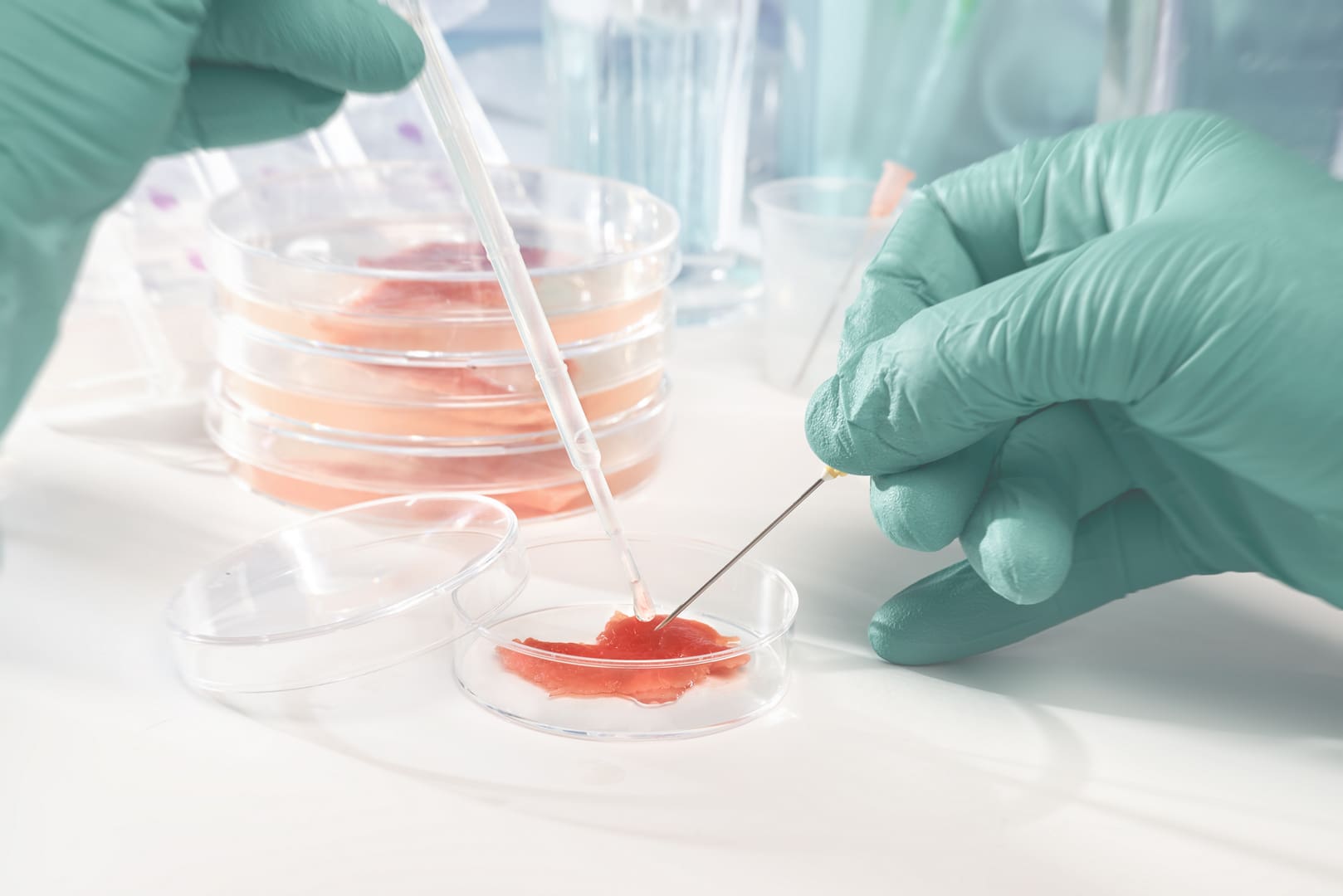
ÖNÜMÜZDEKİ YÜZYILDA YAPAY ETLER REVAÇTA OLACAK
Laboratuvar ortamında artık yapay etler de geliştirilmeye başlandı. Hatta Amerika’da bu ürünler satışa da sunuluyor. Sizce güvenilir mi? Bu tür üretilen ürünler insanların yeme içme alışkanlıklarını ne derece etkileyecek?
Nasıl üretildiğinden başlayarak güvenirliliği konusunda fikir sahibi olabiliriz. Bilimsel araştırmalarda hücre kültürü dediğimiz ortamlarda spesifik hücre tiplerini büyüterek deneyler gerçekleştirebiliyoruz. Hücreyi steril bir petri kabına ekerek uygun aminoasit, besin ve pH koşullarını sağlayarak hayatta kalmasını ve çoğalmasını sağlayabiliyorsunuz. ‘Et nasıl üretiliyor peki?’ derseniz, kök hücreler sayesinde. Kök hücreler tüm hücrelere bölünebilen ata hücreler olup, bu hücreler et üretimi için kas hücrelerine dönüştürülüyor ve trilyonlarca kas hücreleri bir araya gelip dokuyu ve etin yapısını oluşturuyorlar. 2012 yılında ilk çıktığından bir hamburger için gerekli eti üretmek 325 bin dolara mal olmuş. Şu an bu fiyat 10-80 dolar aralığına kadar düşmüş durumda. İnek etinden insanlığı doyurmak için 28 kat daha az alana ve 11 kat daha az suya ihtiyaç duyan bir sistem. Bu sayede küresel ısınma sonucunda maruz kaldığımız ve de gelecek kuşaklarda daha da kötü senaryolarla karşılaşma riskine karşı önemli bir gelişme olarak görülebilir. İnek etinin yerini tutar mı tartışılır. Ancak, maliyetinin düşük olması besin değerlerinin steril laboratuvar ortamlarında kontrol edilebilir olması da önemli. Gelecek kıtlık dönemleri de düşünerek pozitif yaklaşıyorum açıkçası. Tabii tüm genetik kontrollerin yapılarak tüketilmesi önemli. Sadece inek eti değil, tavuk, ördek etlerinin de denemeleri yapılıyor. Gelecek yıllarda besin şeklimiz oldukça değişebilir. Çağ olarak ilginç bir dönemdeyiz. Önümüzdeki yüzyıl çok daha farklı olacak. Dünya nüfusu bu şekilde artmaya devam ederse bu tarz ürünler artarak gelişmeye devam edecek gibi gözüküyor.

GELECEKTE KUSURSUZ İNSAN OLUŞTURULABİLİR
Pandemiden önce Çin’de CRISPR ile süper bebekler geliştirildiği yönünde haberler ortaya çıkmıştı. Bu bebeklerin zeka ve hastalıklar yönünden kusursuz oldukları iddia ediliyordu. Siz bu çalışmaları nasıl değerlendiriyorsunuz? Süper insan yaratmak mümkün mü?
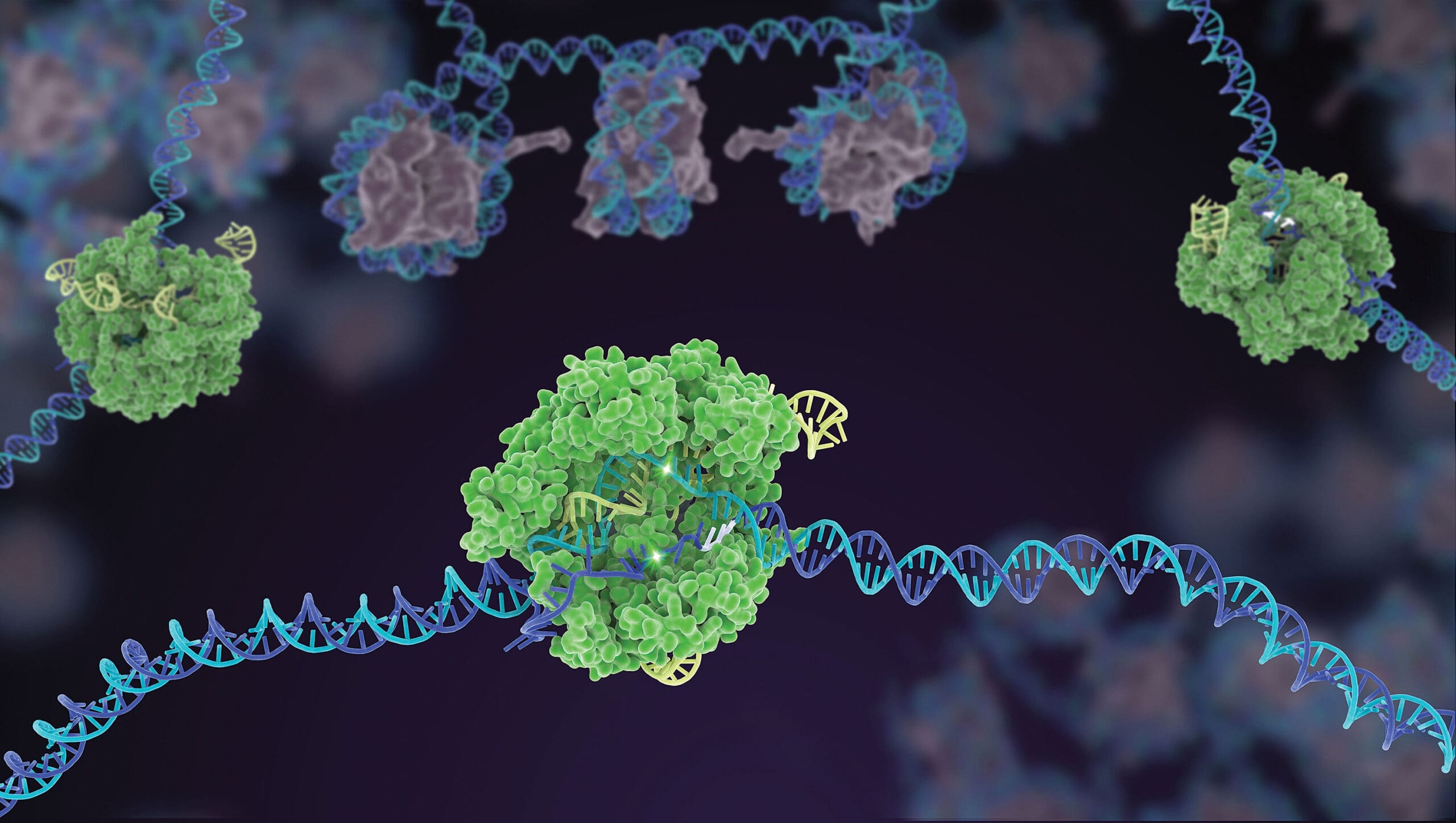
Bu bilgi maalesef yanlış şekilde lanse edildi. CRISPR bebekler HIV’e karşı dirençli olarak He Jiankui tarafından 26 Kasım 2018’de Youtube üzerinden canlı yayınla duyurulmuştur. İkiz bebekler HIV’in bağlandığı receptör olan CRR5 geninde bozukluğa yol açan genetik düzenlemeye embriyo döneminde maruz kaldılar. CRR5 genini seçmesindeki amaç, Avrupa’nın doğusunda yüzde 1’lik popülasyonlu CRR5 geninde 32 bazlık delesyona sahip bireylerin bulunmasıydı. Bu 32 bazlık bölge kişilerde bulunmamasına rağmen sağlıklı ve HIV’e karşı dirençli oldukları tespit edilmişti. Jiankui, bu durumu kullanmak isteyip CRISPR yöntemiyle aynı bölgeyi silmeyi hedeflemiştir. Ancak silmiş olduğu bölgede ayrıca farklı mutasyonların da oluşmasına neden olmuştur. İkiz bebekler Lula ve Nana’nın akıbeti günümüzde bilinmiyor. Jiankui, bu çalışmaları nedeniyle hapse atılmıştı. 3 yıl hapiste kaldıktan sonra geçen yıl nisan ayında serbest bırakılmış, araştırmalarına geri döndüğünü duyurmuştu. Nasıl fonlandığına dair bilgi vermedi ancak, nadir hastalıklarla ilgili genetik tedaviler geliştirmeye çalıştığını açıkladı. Bu tür araştırmaların henüz insan genomunda uygulanması çok tehlikeli. Çünkü off-target olarak adlandırdığımız bilinmeyen gen bölgelerine olası etki, insan hayatına ya da kanser gibi hastalıklara yol açabilir. Tedavi amaçlı kullanılan özel spesifik gene yönelik uygulamaları bu durumun dışında tutuyorum. Bir yumurtayı dölleyerek orada genetik değişimler yapabilecek kadar insan genomunu henüz keşfetmiş durumda değiliz bilim insanları olarak. Tüm gen isimleri bilinse dahi işlevler ve etki mekanizması konularında halen yeni genler bulunmakta, farklı etkileşimler açığa çıkmaktadır. Bu bilinmezlik içerisinde bu tür uygulamaların yapılması oldukça risklidir. Gelecekte bir gün kusursuz insan belki oluşturulabilir. Yakın gelecekte böyle bir şeyin olması henüz pek mümkün gözükmüyor. Kusursuzu da tanımlamak gerekir ama daha da detaya girmek istemiyorum. Vermek istediğim mesaj açıktır umarım.
GENLERİMİZ YAŞANTIMIZI ETKİLİYOR!
Genlerimiz günlük yaşamımızı, yeme içme alışkanlıklarımızı hatta davranış biçimlerimizi etkiliyor mu?
Tabii. Şöyle açıklayabilirim. Genlerin vücudumuzda nasıl aktivite gösterdikleri çok önemli. Cole ve arkadaşları (2020) dilimizdeki test reseptörlerinin ya da sindirim enzimi genlerindeki farklılıkların yiyecekleri sevip sevmememizde etkili olduğunu ortaya çıkarmıştır. Bazı yiyecekleri diğerlerine göre tercih etmenizde etkin rol oynuyor. Tüm etkileşimlerin kimyasal olarak gerçekleşiyor olduğunu düşünürseniz eğer, genetik çeşitliliğimiz bu kimyasal etkilere farklı yanıtlar verebiliyor. Örneğin olfactory reseptör geni özel bir varyanta sahip olanlar beta-ionone kokusunu alabiliyor. Bu kişilerin çay içmeye daha yatkın oldukları tespit edilmiş. Hormonal ve fizyolojik olarak bir çok değişken beslenmenizde ve beslenme alışkanlığınızda etkin rol oynayabilir. Beyninizin ödüllendirme mekanizması psikolojik durumunuzun bozuk olduğu dönemlerde sizi daha fazla enerji kazandıran yiyeceklere yönlendirerek kendinizi daha iyi hissetmenizi sağlarken, bir yandan metabolik olarak yönelimlerinizin değişmesinde etkin rol oynayabilir. (Meraklı araştırmacılar Alonso-Alonso ve arkadaşlarının 2015 çalışmasını inceleyebilir).

ZEKA GENİ ANNEDEN
Türk toplumunda çocuğun iyi ve kötü davranışları anne ya da babayla özelleştirilir. Bir bireyin hangi gen özellikleri anneden, hangi gen özellikleri babadan geçiyor?
Mitokondriye ait DNA’nın anne yumurtasından çocuğa geçtiği bilinmektedir. Anne XX, baba XY kromozomuna sahip olduğu için çocuklarda X kromozomuna bağlı genlerin daha yüksek olasılıkla 2’ye 1 anneden geçtiği düşünülür. Ancak bu sadece bir olasılıktır. Bu nedenle bazı araştırmacılar zekanın X kromozomuna bağlı olduğunu ve daha çok anneye bağlı olabileceğini öne sürmektedirler. Yine tekrar ettiğim üzere bilimsel bir deney sonucunda elde edilmiş veriler değil, gözleme dayalı sonuçlardır. LinRNA H19 isimli genin monoalelik olarak annelerden geçerek kahverengi yağ dokusunda ifade olduğunu ve obeziteye karşı koruma sağladığına dair bir araştırma bulunmaktadır (Schmidt ve arkadaşları 2018). Bir başka araştırmada serotinin seviyesi düşük olan annelerin çocuklarında dikkat dağınıklığı, odaklanamama gibi problemlere maruz kaldığına dair bilgi bulunmaktadır (Halmøy, A. ve arkadaşları 2010). İyi ve kötü davranışların yetiştirilme ve psikolojiyle ilişkilendirilmesi gerektiğini düşünüyorum. Çevresel faktörler, genetikten daha büyük etken bu konuda.

ÇOK SAYIDA BİYOLOG VE MOLEKÜLER BİYOLOĞA İHTİYAÇ VAR
Türkiye’de moleküler biyoloji nereye gidiyor?
Türkiye’de moleküler biyoloji kan kaybediyor. Çok önemli cevher olabilecek, ülke ekonomisine önemli katkılar sunabilecek gençlerimize fırsat yaratma ve onlara araştırma imkanı verme konusunda yetersiz bir ülkedeyiz. Bu nedenle çoğu başarılı genç bu alanda yurt dışında araştırmalarına devam ediyor. Destek miktarları yeterli değil maalesef. Biyoteknoloji alanında önemli bir yatırım yapılması gerekiyor. Gençlerimiz işsiz kalıyorlar. Çalışabilecekleri iş alanları çok kısıtlı. Bu nedenle gelecek görülmediği için ÖSYM sınav puanlarında da yerleştirmelerde düşüşler devam ediyor. Çok fazla alanda yetkin biyolog ve moleküler biyologlara ihtiyacımız olmasına rağmen onlara doğru iş modellerini oluşturamadığımız için bu alana ilgi duyan gençler yurt dışını hedef almaktalar. İş veren ‘biyolog ne yapar ki?’ diye düşünüyor. Etkinliğine dair yeterli toplum bilgisine ulaşmamız şart. Bitki, hayvan, insan genom araştırmaları, çevre, iklim değişikliği, su kirliliği, tarım, havacılık, uzay araştırmaları konularında biyologların etkin rol oynaması gerekirken sosyal algı nedeniyle bu arkadaşlarımız geri planda kalıyor. Moleküler biyologlar hastanelerde cihaz başında çalışıp sonuç veren kişiler değildir. Toplumumuzda bu algının kırılması gerekiyor. Moleküler biyologlar az önce anlattığım tüm konularda alanlarında uzmanlaşarak fikir sahibi olabilir. Bitki-hayvan-insan hücre metabolizmasından genetiğine, hastanelerde kullanılan kan değerlerini ölçen kitlerin oluşturulmasına, koronavirüs gibi viral hastalıkların tespit edilmesi için genetik analizlerin yapılmasına, hastalıkların genetik test analizlerinin gerçekleştirilmesine kadar daha sayamadığım birçok konuda etkin rol oynayabilecek donanımlı bireylerdir. Toplumumuzda bir gün mesleğimizin saygınlık kazanmasını umut ediyorum.

Son çalışmalarınızdan bize bahseder misiniz?
TÜBİTAK 2214 programı ile doktora çalışmalarımı Amerika’da Asistant. Prof. Dr. Önder Albayram ile birlikte nörodejeneratif hastalıklarda beyin enerji metabolizmasının önemi üzerinde gerçekleştirdim. Şu an önemli bulgular duyuracağımız çalışmalarımızı hazırlama aşamasındayız. O nedenle yayınlanmadan detay veremeyeceğim henüz. Genom analizi ile ilgili bir şirket kurmak üzerine çalışmamız var şu an. Hastaların genom bilgilerini inceleyerek doğru mutasyon tespitlerini gerçekleştirdiğimiz kendi yazılımımızı oluşturduk. Yoğun bir şekilde tüm süreçleri yönetmeye çalışıyorum diyebilirim.